Postulados:
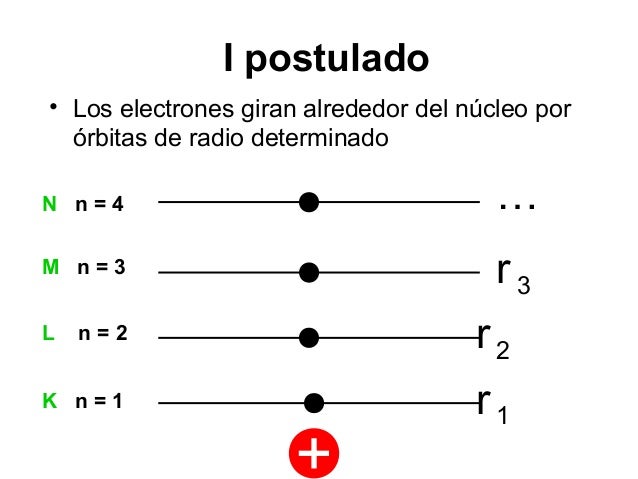
1. Primer Postulado: Estabilidad del Electrón
Un electrón en un átomo se mueve en una órbita circular alrededor del núcleo bajo
la influencia de la atracción entre el electrón y el núcleo, obedeciendo las leyes de
la mecánica clásica.
Las únicas fuerzas que actúan sobre el electrón son las fuerzas de atracción
eléctrica (Fa) y la fuerza centrípeta (Fc), que es exactamente igual a la fuerza
centrífuga.
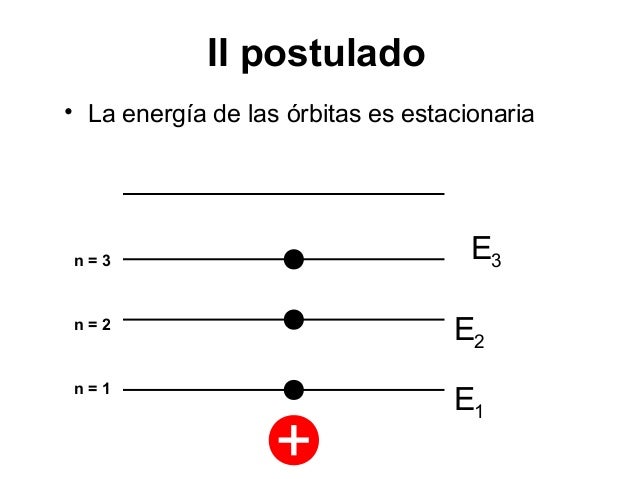
2. Segundo Postulado: Orbitas o niveles permitidos
En lugar de la infinidad de órbitas posibles en la mecánica clásica, para un
electrón solo es posible moverse en una órbita para la cual el momento angular
L es un múltiplo entero de la constante de Planck h.
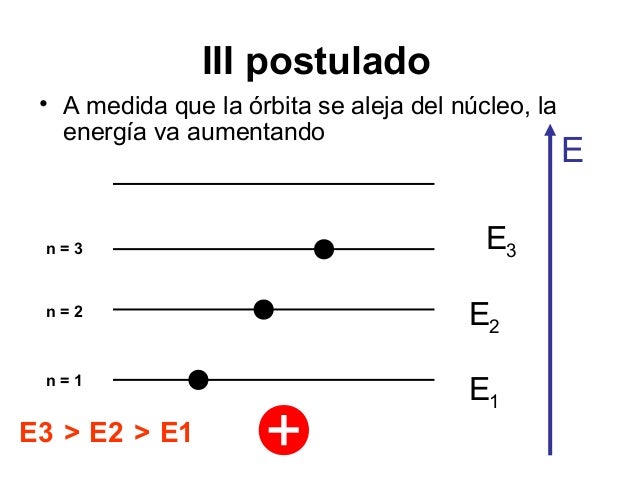
3. Tercer Postulado: Niveles Estacionarios de Energía
Un electrón que se mueva en una de esas órbitas permitidas no irradia energía
electromagnética, aunque está siendo acelerado constantemente por las fuerzas
atractivas al núcleo. Por ello, su energía total permanece constante.
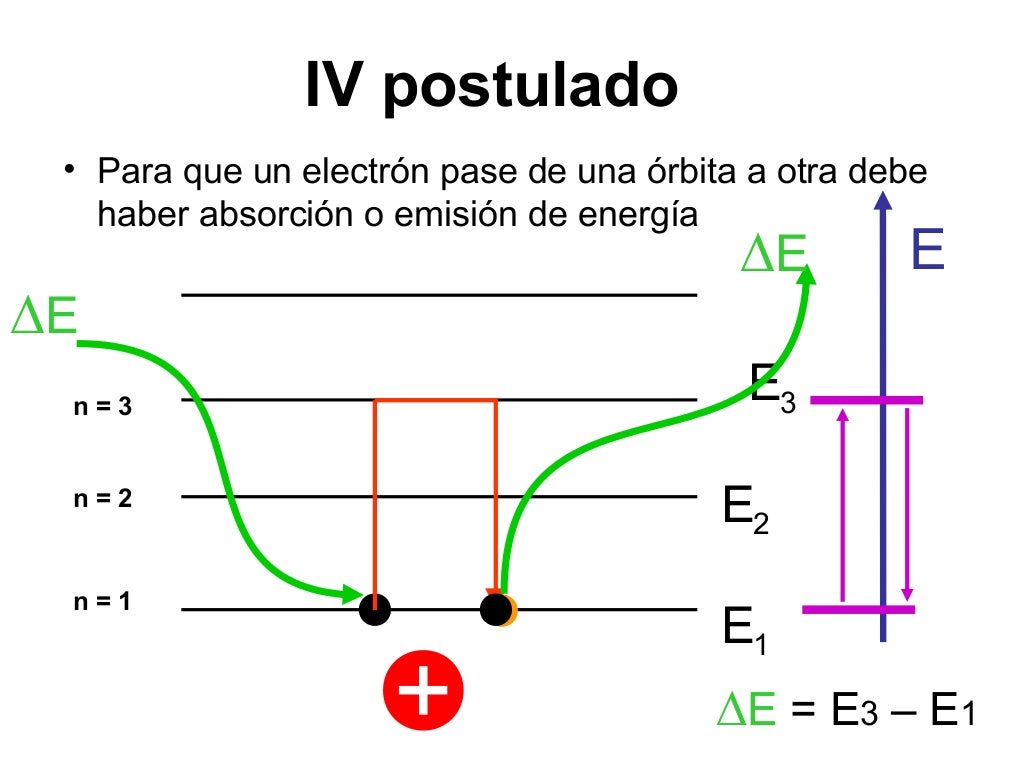
4. Cuarto Postulado: Emisión y Absorción de Energía
Si un electrón que inicialmente se mueve en una órbita de energía Ei cambia
discontinuamente su movimiento de forma que pasa a otra órbita de energía Ef se
emite o absorbe energía electromagnética para compensar el cambio de la
energía total. La frecuencia ν de la radiación es igual a la cantidad (Ei – Ef)
dividida por la constante de Planck h.

Un cordial saludo. Asumiendo que el tema puede resultar de interés profesional, les cuento lo siguiente; con respecto a la unidad de medida de la Constante de Planck y las hipótesis sobre "la posible presencia de variables ocultas en los fundamentos conceptuales de la Mecánica Cuántica", resulta que tanto el Programa de Inteligencia Artificial de Microsoft "Copilot" como "ChatGpt" de Google han deducido matemáticamente! (o sea, no basado en nuevas hipótesis y/o interpretaciones teóricas) que "existe una magnitud física OCULTA en la conocida unidad de medida de la Constante de Planck, y que al ser considerada permite resolver problemas teóricos-conceptuales pendientes de solución en la Mecánica Cuántica"!. Por lo trascendental de este resultado, y porque se trata de una demostración basada en cálculos matemáticos prácticamente triviales (por lo tanto, convincentes!) evidentemente resulta un tema de marcado interés científico analizar seriamente la veracidad o no de este resultado. Si les resulta de interés analizar estos resultados hacédmelo saber a mi dirección e-mail para enviarles los textos. Atentamente, José Alberto
ResponderBorrar